1. Introduction
Nuclear medicine is an interdisciplinary field integrating nuclear physics, radiochemistry, medical instrumentation engineering, pharmaceutical science, and clinical medicine to generate functional and molecular information about biological systems through the administration of radiopharmaceuticals. This distinguishes nuclear medicine fundamentally from anatomical imaging modalities such as computed tomography (CT) and magnetic resonance imaging (MRI), which primarily depict structural morphology.
The central strength of nuclear medicine lies not merely in radiation-based image formation, but in the selective use of radionuclides and biologically targeted carrier molecules that enable visualization of physiological processes, metabolic pathways, and molecular expression patterns in vivo. Consequently, the performance of a nuclear medicine system depends not only on the imaging instrument itself, but on the broader technological ecosystem encompassing radionuclide production, radiopharmaceutical preparation, product distribution, imaging instrumentation, data processing, infrastructure, and specialized personnel.
From a systems perspective, modern clinical nuclear medicine may be broadly categorized into two principal architectural paradigms:
(1) Generator-based conventional nuclear medicine platforms, and
(2) Cyclotron-based positron emission tomography (PET) molecular imaging platforms.
Tc-99m and F-18 serve as representative radionuclides of these two paradigms, respectively.
Although both platforms can be applied to skeletal imaging, bone imaging represents only one among many applications supported by each platform and was not the sole driving purpose of their technological development. Therefore, comparing Tc-99m bone scintigraphy and F-18 NaF PET solely as “bone imaging modalities” may inadequately capture the broader architectural and strategic distinctions between these two nuclear medicine systems.
This article therefore presents a comparative analysis of Tc-99m and F-18 PET platforms from the perspectives of production architecture, imaging physics, infrastructure requirements, clinical applications, and healthcare system integration, using skeletal imaging as a representative case study to illustrate the differing design philosophies underlying these two nuclear medicine paradigms.
2. The Tc-99m Platform: Generator-Based Conventional Nuclear Medicine System
2.1 Fundamental Properties of Tc-99m and Its Suitability for Clinical Imaging
Technetium-99m (Tc-99m) is a gamma-emitting radionuclide widely recognized as the principal workhorse of conventional nuclear medicine, accounting for the majority of diagnostic nuclear medicine procedures worldwide.
Tc-99m has a physical half-life of approximately 6.01 hours, a duration highly favorable for clinical use because it is sufficiently long to permit radiopharmaceutical preparation, in-hospital distribution, and patient imaging, yet short enough to minimize residual radiation burden following administration.
Additionally, Tc-99m emits a principal gamma photon at approximately 140.5 keV, an energy range well suited for detection by scintillation detectors such as sodium iodide activated with thallium [NaI(Tl)], providing an advantageous balance between photon penetration through tissue and detector efficiency.
Furthermore, Tc-99m emits negligible charged particle radiation of biological significance, thereby minimizing absorbed dose to patient tissues relative to many alternative radionuclides.
Collectively, these characteristics render Tc-99m one of the closest practical approximations to an ideal diagnostic radionuclide for gamma camera imaging in conventional nuclear medicine.
2.2 Mo-99/Tc-99m Production and Generator-Based Distribution Architecture
Despite its favorable imaging properties, the short half-life of Tc-99m precludes efficient long-distance shipment as a ready-to-use radiopharmaceutical. To overcome this limitation, nuclear medicine adopted the radionuclide generator concept.
Tc-99m is obtained through decay of molybdenum-99 (Mo-99), which has a half-life of approximately 66 hours and is produced primarily via fission of uranium-235 in research or isotope production reactors:
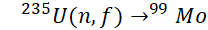
Produced Mo-99 is loaded into Mo-99/Tc-99m generators, typically adsorbed onto alumina columns. As Mo-99 decays, Tc-99m is generated in the form of pertechnetate and can be eluted using sterile saline for subsequent radiopharmaceutical preparation.
This architecture constitutes one of the most important systemic innovations in the history of nuclear medicine, as it transforms the logistical challenge of distributing short-lived radionuclides into a practical on-site radionuclide generation model.
The resulting distributed radionuclide deployment architecture enables broad dissemination of nuclear medicine services to hospitals without requiring local reactors or accelerators.
2.3 Chemical Flexibility and the Role of Tc-99m as a Radiopharmaceutical Platform
Beyond logistical advantages, Tc-99m possesses highly favorable coordination chemistry that enables formation of stable complexes with a broad range of ligands, facilitating development of diverse targeted radiopharmaceuticals.
Tc-99m can be incorporated into compounds including phosphonates, iminodiacetic acid derivatives, sestamibi, DMSA, MAG3, nanocolloids, and peptide-based tracers, thereby enabling imaging of multiple organ systems.
This chemical versatility establishes Tc-99m not merely as a radionuclide for skeletal imaging, but as the chemical and clinical foundation of the broader conventional nuclear medicine platform.
2.4 Clinical Applications of the Tc-99m Platform
The Tc-99m platform supports a wide spectrum of clinical imaging applications, including:
- Skeletal imaging using phosphonate compounds
- Myocardial perfusion imaging using Tc-99m sestamibi or tetrofosmin
- Renal functional imaging using Tc-99m DTPA, MAG3, or DMSA
- Hepatobiliary imaging using HIDA derivatives
- Pulmonary ventilation-perfusion imaging
- Sentinel lymph node mapping
- Thyroid and salivary gland imaging
Accordingly, skeletal imaging represents only one of numerous major clinical applications of the Tc-99m platform rather than its sole purpose.
3. The F-18 PET Platform: Cyclotron-Based Molecular Imaging System
3.1 Fundamental Properties of F-18 and Its Suitability for PET Imaging
Fluorine-18 (F-18) is the most widely utilized positron-emitting radionuclide in PET imaging due to its highly favorable physical properties for high-resolution molecular imaging.
F-18 has a physical half-life of approximately 109.8 minutes, sufficiently long for radiopharmaceutical synthesis, quality control, and regional distribution, yet short enough to maintain acceptable radiation exposure profiles.
F-18 emits positrons with a maximum energy of approximately 0.635 MeV, which is relatively low compared with many other positron emitters. This reduces positron range in tissue prior to annihilation, thereby improving spatial localization and image resolution.
These properties make F-18 the radionuclide of choice for many molecular imaging applications in both clinical practice and research.
3.2 Cyclotron Production of F-18 and Infrastructure Requirements
Unlike Tc-99m, F-18 must be produced directly using a cyclotron via the nuclear reaction:
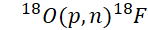
This reaction is performed using enriched [18O] water targets irradiated with high-energy protons.
Production of F-18 requires substantially more complex infrastructure than the Tc-99m platform, including:
- Medical cyclotrons
- Targetry and thermal management systems
- Shielded hot cells
- Automated synthesis modules
- Radiopharmaceutical quality control laboratories
- Good Manufacturing Practice (GMP)-compliant production environments
Consequently, operation of the F-18 PET platform requires multidisciplinary teams including cyclotron engineers, radiochemists, radiopharmacists, medical physicists, and quality assurance personnel.
3.3 PET Imaging Principles and Detector System Advantages
PET differs fundamentally from gamma camera/SPECT imaging in its detection physics.
Following radioactive decay, F-18 emits a positron, which loses kinetic energy in tissue before annihilating with an electron. This annihilation event produces two 511 keV photons emitted in approximately opposite directions.
PET systems detect these photons simultaneously using coincidence detection and reconstruct the line-of-response corresponding to the annihilation event.
A major advantage of PET is that it does not require collimation, unlike gamma camera/SPECT systems. This dramatically improves photon utilization efficiency, resulting in:
- Higher detection sensitivity
- Superior spatial resolution
- Enhanced quantitative imaging capability
However, PET remains subject to its own physical limitations, including positron range, photon non-collinearity, and detector timing resolution constraints.
3.4 Principal Clinical Role of the PET Platform in Modern Nuclear Medicine
Although PET can be applied to skeletal imaging, it was not developed primarily for bone imaging. Rather, PET was designed to support metabolic and molecular imaging applications beyond the capabilities of conventional nuclear medicine.
Its most important clinical application is F-18 fluorodeoxyglucose (FDG) PET, which has become a cornerstone of modern oncology for:
- Cancer staging
- Metastatic disease assessment
- Therapy response monitoring
- Recurrence detection
PET also plays major roles in:
- Brain imaging for neurodegenerative and neurological disorders
- Cardiac metabolic imaging
- Inflammation imaging
- Targeted receptor and molecular pathway imaging
Thus, PET should be understood primarily as an advanced molecular imaging platform rather than as a dedicated skeletal imaging technology.
3.5 Application of F-18 PET to Skeletal Imaging
For skeletal imaging, PET commonly employs F-18 sodium fluoride (F-18 NaF), which accumulates in bone through exchange of fluoride ions with hydroxyl groups in hydroxyapatite, producing fluorapatite-like surface binding.
This mechanism makes F-18 NaF highly sensitive to areas of increased osteoblastic activity and bone remodeling.
However, in healthcare system practice, F-18 NaF PET is generally implemented as an additional application of existing PET infrastructure rather than as the primary justification for PET installation.
Accordingly, F-18 NaF PET should be viewed as a specialized skeletal application of the broader PET molecular imaging platform rather than as an independently developed bone imaging technology.
4. Skeletal Imaging as a Comparative Case Study of Tc-99m and F-18 PET Platforms
Skeletal imaging provides an appropriate case study for comparing the Tc-99m and F-18 PET platforms because both systems can evaluate similar physiological processes in bone while operating through fundamentally different radionuclide production architectures, detection physics, and clinical infrastructures.
In this context, the comparison between Tc-99m bone scintigraphy and F-18 NaF PET is not intended to determine which modality is universally “superior,” but rather to illustrate how differences in nuclear medicine platform architecture translate into distinct performance characteristics, operational constraints, and clinical deployment strategies.
4.1 Tc-99m Bone Scintigraphy: Application of the Conventional Nuclear Medicine Platform for Skeletal Assessment
Tc-99m bone scintigraphy is one of the most widely utilized applications of the Tc-99m platform. It commonly employs phosphonate-based radiopharmaceuticals such as Tc-99m MDP, Tc-99m HDP, and Tc-99m HMDP, which bind to the surface of hydroxyapatite crystals in bone, particularly in regions of active bone formation and elevated osteoblastic activity.
Accordingly, tracer uptake on bone scintigraphy primarily reflects bone remodeling activity rather than direct anatomical bone structure.
This characteristic renders Tc-99m bone scintigraphy highly sensitive to pathological processes associated with altered bone turnover, including metastatic bone disease, osteomyelitis, stress fractures, and metabolic bone disorders.
Because of its favorable cost profile, broad availability, and ability to accommodate high patient throughput, Tc-99m bone scintigraphy has become the standard modality for routine skeletal imaging in many healthcare systems.
4.2 F-18 NaF PET Bone Imaging: Application of the Molecular Imaging Platform for Skeletal Assessment
F-18 NaF PET represents the application of the PET platform to skeletal imaging through the use of F-18 sodium fluoride, which accumulates in bone via exchange of fluoride ions with hydroxyl groups in hydroxyapatite crystals.
This mechanism makes F-18 NaF highly sensitive to regions of increased osteoblastic activity in a manner analogous to Tc-99m bone-seeking agents. However, when combined with the PET platform, which possesses inherently superior detection performance, it enables skeletal imaging with greater sensitivity and higher spatial resolution.
Clinically, F-18 NaF PET is typically employed in scenarios requiring enhanced sensitivity or specificity for skeletal lesion assessment, such as complex metastatic bone disease evaluation, equivocal findings on conventional bone scintigraphy, or quantitative follow-up in research and precision medicine settings.
Nevertheless, such applications generally occur in centers where PET infrastructure is already available, rather than as justification for dedicated PET installation solely for skeletal imaging.
4.3 Physical Performance Comparison of Bone Scintigraphy and Bone PET
Although both technologies assess similar bone remodeling processes, their imaging performance differs substantially due to the fundamental physics of their respective detection systems.
Tc-99m bone scintigraphy relies on gamma photon detection through a collimator, which constitutes an inherent limitation of gamma camera/SPECT systems because most emitted photons must be rejected in order to preserve spatial information, thereby substantially reducing detection efficiency.
Spatial resolution is further constrained by collimator geometry, detector-to-patient distance, septal penetration, and photon scatter.
In contrast, PET employs coincidence detection without collimation, resulting in inherently higher sensitivity and superior spatial resolution. PET also supports quantitative analysis through parameters such as standardized uptake value (SUV).
Accordingly, from a detector physics perspective, F-18 NaF PET offers clear advantages over Tc-99m bone scintigraphy in lesion detectability, spatial resolution, and quantitative imaging capability.
However, these advantages reflect detector platform performance rather than universal clinical superiority in all practice settings.
5. Infrastructure and Supply Chain Comparison of the Two Platforms
Beyond imaging performance, one of the most significant distinctions between the Tc-99m and F-18 PET platforms lies in the infrastructure architecture and supply chain required to support their operation.
The Tc-99m platform is based on a centralized production with decentralized clinical deployment model. Mo-99 is produced in nuclear reactors at national or regional facilities and distributed to hospitals in the form of Mo-99/Tc-99m generators, allowing Tc-99m to be prepared locally at the point of care.
In contrast, the F-18 PET platform depends on a regional advanced production network consisting of cyclotron facilities, radiopharmaceutical synthesis laboratories, quality control systems, and rapid transportation logistics operating within the constraints of short radionuclide half-life.
Thus, Tc-99m and F-18 PET represent fundamentally different healthcare delivery architectures in terms of centralization, operational complexity, and infrastructure requirements.
6. Resource Allocation and Healthcare Economics Considerations
In real-world healthcare systems, selection of nuclear medicine technology is not determined solely by technical imaging performance but by the balance between cost and clinical value.
The Tc-99m platform offers substantial advantages in healthcare economics due to its lower infrastructure requirements, simpler radiopharmacy workflow, reduced staffing complexity, and ability to support high patient throughput at relatively low per-scan cost.
Conversely, PET/CT represents a high-cost resource in terms of instrumentation, infrastructure, and operational expenditure, and is therefore typically prioritized for clinical indications where molecular imaging provides substantial incremental value in patient management.
Consequently, although F-18 NaF PET provides superior skeletal imaging performance, its routine use as a general skeletal imaging modality may not represent the most resource-efficient strategy in many healthcare systems.
7. Strategic Design of Tiered Nuclear Medicine Service Models
Given these differences in performance, infrastructure, and cost, Tc-99m and PET should not be viewed as directly competing technologies within healthcare systems. Rather, they should be considered complementary components of a tiered nuclear medicine service model.
Within such a framework, the Tc-99m platform serves as a frontline broad-access nuclear imaging platform for high-volume general imaging applications requiring widespread accessibility.
By contrast, the PET platform functions as an advanced molecular imaging referral platform for specialized applications demanding greater sensitivity, specificity, or quantitative capability.
Within this framework, F-18 NaF PET should be positioned as an advanced skeletal imaging application of the PET platform rather than as a direct replacement for Tc-99m bone scintigraphy.
8. Conclusion
Tc-99m and F-18 PET should not be regarded merely as two radionuclides used for nuclear imaging, but rather as representatives of two fundamentally different architectural paradigms in modern nuclear medicine systems.
The Tc-99m platform reflects a decentralized imaging model optimized for broad accessibility, cost-efficiency, and high clinical throughput.
In contrast, the F-18 PET platform reflects an advanced molecular imaging paradigm optimized for imaging performance, detection sensitivity, and quantitative capability within more specialized and infrastructure-intensive clinical settings.
The skeletal imaging case study demonstrates that although F-18 NaF PET offers superior physical imaging performance compared with Tc-99m bone scintigraphy in several respects, this advantage does not imply that PET was designed to replace the Tc-99m platform for skeletal imaging. Rather, it reflects that skeletal imaging is only one of many specialized applications supported by the broader PET molecular imaging platform.
Accordingly, comparison between Tc-99m bone scintigraphy and F-18 NaF PET should be interpreted as a comparison between two skeletal imaging applications derived from fundamentally different nuclear medicine platform architectures, rather than as a direct technological competition between two isolated bone imaging modalities.
*****************************************************************************
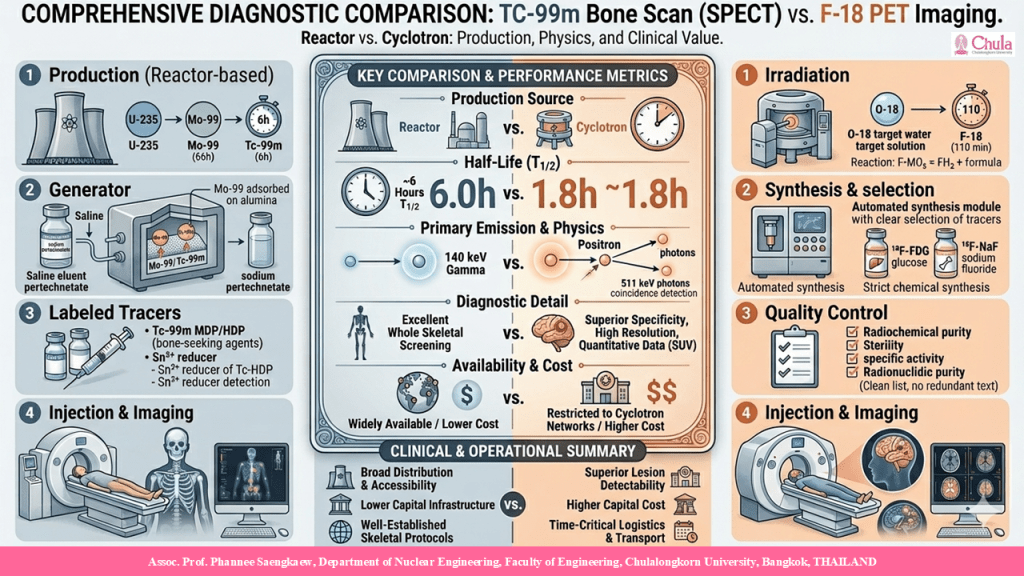
การวิเคราะห์เปรียบเทียบแพลตฟอร์มเวชศาสตร์นิวเคลียร์ Tc-99m SPECT และ F-18 PET
1. บทนำ
เวชศาสตร์นิวเคลียร์เป็นศาสตร์สหวิทยาการที่บูรณาการองค์ความรู้ด้านฟิสิกส์นิวเคลียร์ เคมีรังสี วิศวกรรมเครื่องมือแพทย์ เภสัชศาสตร์ และเวชศาสตร์คลินิก เพื่อสร้างข้อมูลเชิงหน้าที่และระดับโมเลกุลของระบบชีวภาพผ่านการให้สารเภสัชรังสีแก่ผู้ป่วย ซึ่งแตกต่างโดยพื้นฐานจากเทคนิคการสร้างภาพเชิงกายวิภาค เช่น เอกซเรย์คอมพิวเตอร์ (Computed Tomography; CT) และการสร้างภาพด้วยคลื่นแม่เหล็กไฟฟ้า (Magnetic Resonance Imaging; MRI) ที่มุ่งแสดงลักษณะทางสัณฐานวิทยาของอวัยวะเป็นหลัก
จุดแข็งสำคัญของเวชศาสตร์นิวเคลียร์มิได้อยู่เพียงที่การสร้างภาพจากการปล่อยรังสี หากแต่อยู่ที่การเลือกใช้ไอโซโทปกัมมันตรังสีร่วมกับสารพาหะทางชีวภาพที่มีความจำเพาะ เพื่อให้สามารถแสดงกระบวนการทางสรีรวิทยา วิถีเมแทบอลิซึม และการแสดงออกของโมเลกุลต่าง ๆ ภายในร่างกายได้โดยตรง ดังนั้น สมรรถนะของระบบเวชศาสตร์นิวเคลียร์จึงมิได้ขึ้นกับเครื่องสร้างภาพเพียงอย่างเดียว แต่ขึ้นกับระบบเทคโนโลยีโดยรวม ซึ่งครอบคลุมตั้งแต่การผลิตไอโซโทปกัมมันตรังสี การเตรียมสารเภสัชรังสี การกระจายผลิตภัณฑ์ เครื่องมือสร้างภาพ การประมวลผลข้อมูล ตลอดจนโครงสร้างพื้นฐานและบุคลากรเฉพาะทาง
ในมุมมองเชิงระบบ เวชศาสตร์นิวเคลียร์ทางคลินิกสมัยใหม่สามารถจำแนกได้เป็นสองสถาปัตยกรรมหลัก ได้แก่
(1) แพลตฟอร์มเวชศาสตร์นิวเคลียร์แบบดั้งเดิมที่อาศัยเครื่องกำเนิดรังสีเป็นฐาน และ
(2) แพลตฟอร์มการสร้างภาพระดับโมเลกุลแบบไซโคลตรอนและเอกซเรย์ปล่อยโพซิตรอนเป็นฐาน
โดยมี Tc-99m และ F-18 เป็นไอโซโทปตัวแทนของแต่ละสถาปัตยกรรมตามลำดับ
แม้ว่าทั้งสองแพลตฟอร์มจะสามารถประยุกต์ใช้ในการตรวจสแกนกระดูกได้ แต่การสร้างภาพระบบกระดูกเป็นเพียงหนึ่งในหลายการประยุกต์ใช้ของแต่ละแพลตฟอร์ม และมิใช่วัตถุประสงค์หลักเพียงประการเดียวที่ขับเคลื่อนการพัฒนาเทคโนโลยีเหล่านี้ ดังนั้น การเปรียบเทียบ Tc-99m Bone Scintigraphy และ F-18 NaF PET โดยมองเพียงว่าเป็น “เทคโนโลยีตรวจสแกนกระดูก” อาจไม่เพียงพอที่จะสะท้อนความแตกต่างเชิงสถาปัตยกรรมและเชิงยุทธศาสตร์ของระบบเวชศาสตร์นิวเคลียร์ทั้งสอง
บทความนี้จึงมุ่งวิเคราะห์เปรียบเทียบแพลตฟอร์ม Tc-99m และ F-18 PET ในมิติของสถาปัตยกรรมการผลิตไอโซโทป ฟิสิกส์การสร้างภาพ โครงสร้างพื้นฐาน การประยุกต์ใช้ทางคลินิก และการบูรณาการเข้าสู่ระบบสุขภาพ โดยใช้การสร้างภาพระบบกระดูกเป็นกรณีศึกษาเชิงตัวแทนเพื่อสะท้อนให้เห็นถึงปรัชญาการออกแบบที่แตกต่างกันของแพลตฟอร์มเวชศาสตร์นิวเคลียร์ทั้งสอง
2. แพลตฟอร์ม Tc-99m: ระบบเวชศาสตร์นิวเคลียร์แบบดั้งเดิมที่อาศัยเครื่องกำเนิดรังสี
2.1 คุณสมบัติพื้นฐานของ Tc-99m และความเหมาะสมต่อการสร้างภาพทางคลินิก
เทคนีเชียม-99m (Technetium-99m; Tc-99m) เป็นไอโซโทปกัมมันตรังสีชนิดปล่อยรังสีแกมมาที่ได้รับการยอมรับอย่างกว้างขวางว่าเป็นไอโซโทปหลักของเวชศาสตร์นิวเคลียร์แบบดั้งเดิม และมีสัดส่วนการใช้งานสูงที่สุดในบรรดาการตรวจเวชศาสตร์นิวเคลียร์ทั่วโลก
Tc-99m มีครึ่งชีวิตทางกายภาพประมาณ 6.01 ชั่วโมง ซึ่งเหมาะสมอย่างยิ่งต่อการใช้งานทางคลินิก เนื่องจากยาวพอสำหรับการเตรียมสารเภสัชรังสี การขนส่งภายในโรงพยาบาล และการดำเนินการตรวจผู้ป่วย ขณะเดียวกันก็สั้นพอที่จะลดภาระรังสีตกค้างหลังการตรวจ
นอกจากนี้ Tc-99m ปล่อยโฟตอนแกมมาหลักที่พลังงานประมาณ 140.5 กิโลอิเล็กตรอนโวลต์ ซึ่งเหมาะสมต่อการตรวจวัดด้วยหัววัดรังสีชนิดผลึกเรืองแสง เช่น โซเดียมไอโอไดด์เจือแทลเลียม [NaI(Tl)] โดยให้สมดุลที่เหมาะสมระหว่างความสามารถในการทะลุผ่านเนื้อเยื่อและประสิทธิภาพการตรวจวัดของหัววัดรังสีอีกทั้ง Tc-99m แทบไม่มีการปล่อยอนุภาคมีประจุที่มีนัยสำคัญทางชีวภาพ จึงช่วยลดปริมาณรังสีดูดกลืนต่อผู้ป่วยเมื่อเทียบกับไอโซโทปหลายชนิด ด้วยคุณสมบัติดังกล่าว Tc-99m จึงถือเป็นหนึ่งในไอโซโทปที่ใกล้เคียงกับ “ไอโซโทปวินิจฉัยในอุดมคติ” มากที่สุดสำหรับการสร้างภาพด้วยกล้องแกมมาในเวชศาสตร์นิวเคลียร์แบบดั้งเดิม
2.2 การผลิต Mo-99/Tc-99m และสถาปัตยกรรมการกระจายแบบเครื่องกำเนิดรังสี
Tc-99m ได้จากการสลายตัวของนิวไคลด์แม่ (Parent Nuclide) คือ โมลิบดีนัม-99 (Mo-99) ซึ่งเป็นผลผลิตจากปฏิกิริยาฟิชชันของยูเรเนียม-235
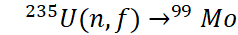
ภายในเครื่องปฏิกรณ์นิวเคลียร์วิจัยหรือเครื่องปฏิกรณ์ผลิตไอโซโทป (Isotope Production Reactor)
กระบวนการดังกล่าวให้ Mo-99 ที่มีกัมมันตภาพจำเพาะสูง (High-Specific-Activity) ซึ่งเหมาะสำหรับการผลิตเครื่องกำเนิดรังสีเชิงพาณิชย์
แม้ Tc-99m จะมีคุณสมบัติทางภาพที่เหมาะสม แต่ครึ่งชีวิตที่สั้นทำให้ไม่สามารถขนส่งระยะไกลในรูปสารเภสัชรังสีพร้อมใช้ได้อย่างมีประสิทธิภาพ ดังนั้น เวชศาสตร์นิวเคลียร์จึงพัฒนาแนวคิด “เครื่องกำเนิดรังสี” ขึ้นเพื่อแก้ปัญหาดังกล่าว
Tc-99m ได้จากการสลายตัวของโมลิบดีนัม-99 (Mo-99) ซึ่งมีครึ่งชีวิตประมาณ 66 ชั่วโมง และผลิตหลักผ่านกระบวนการฟิชชันของยูเรเนียม-235 ภายในเครื่องปฏิกรณ์วิจัยหรือเครื่องปฏิกรณ์ผลิตไอโซโทป Mo-99 ที่ผลิตได้จะถูกบรรจุลงในเครื่องกำเนิดรังสี Mo-99/Tc-99m โดยตรึงบนคอลัมน์อะลูมินา เมื่อ Mo-99 สลายตัวจะให้ Tc-99m ในรูปเพอร์เทคนีเทต ซึ่งสามารถชะออกด้วยน้ำเกลือปราศจากเชื้อเพื่อนำไปเตรียมสารเภสัชรังสีต่อ
สถาปัตยกรรมดังกล่าวถือเป็นหนึ่งในนวัตกรรมเชิงระบบที่สำคัญที่สุดในประวัติศาสตร์เวชศาสตร์นิวเคลียร์ เนื่องจากเปลี่ยนข้อจำกัดของการกระจายไอโซโทปครึ่งชีวิตสั้นให้กลายเป็นระบบการสร้างไอโซโทป ณ จุดใช้งานได้จริง ผลลัพธ์คือการเกิดเครือข่ายกระจายไอโซโทปแบบกระจายศูนย์ ซึ่งช่วยให้โรงพยาบาลจำนวนมากสามารถให้บริการเวชศาสตร์นิวเคลียร์ได้โดยไม่ต้องมีเครื่องปฏิกรณ์หรือเครื่องเร่งอนุภาคประจำสถานที่ นี่คือเหตุผลสำคัญที่ทำให้ Tc-99m มีการใช้งานแพร่หลายทั่วโลก
2.3 ความยืดหยุ่นทางเคมีและบทบาทของ Tc-99m ในฐานะแพลตฟอร์มสารเภสัชรังสี
นอกเหนือจากข้อได้เปรียบด้านโลจิสติกส์ Tc-99m ยังมีคุณสมบัติทางเคมีเชิงประสานที่เหมาะสมอย่างยิ่ง ทำให้สามารถสร้างสารเชิงซ้อนที่เสถียรกับลิแกนด์หลากหลายชนิด และเอื้อต่อการพัฒนาสารเภสัชรังสีที่มีเป้าหมายจำเพาะหลายรูปแบบ
Tc-99m สามารถใช้ติดฉลากกับสารประกอบได้หลากหลาย เช่น phosphonates, iminodiacetic acid derivatives, sestamibi, DMSA, MAG3, nanocolloids และ peptide-based tracers ส่งผลให้สามารถใช้สร้างภาพได้กับหลายระบบอวัยวะ สรุป คือ Tc-99m Pertechnetate จะถูกติดฉลากรังสี (Radiolabel) กับลิแกนด์ฟอสโฟเนต (Phosphonate Ligands) เช่น
- Tc-99m-MDP
- Tc-99m-HDP
- Tc-99m-HMDP
สารเหล่านี้มีความชอบจับ (Affinity) ต่อพื้นผิวผลึกไฮดรอกซีอะพาไทต์ โดยเฉพาะบริเวณที่มีการสร้างกระดูกอย่างต่อเนื่อง (Active Osteogenesis)
ดังนั้น ความยืดหยุ่นทางเคมีนี้จึงทำให้ Tc-99m มิใช่เพียงไอโซโทปสำหรับการตรวจสแกนกระดูก หากแต่เป็นรากฐานทางเคมีและทางคลินิกของแพลตฟอร์มเวชศาสตร์นิวเคลียร์แบบดั้งเดิมโดยรวม
2.4 การประยุกต์ใช้ทางคลินิกของแพลตฟอร์ม Tc-99m
แพลตฟอร์ม Tc-99m รองรับการสร้างภาพทางคลินิกได้อย่างกว้างขวาง ได้แก่
- การตรวจสแกนกระดูกด้วยสารกลุ่ม phosphonate
- การตรวจการไหลเวียนเลือดกล้ามเนื้อหัวใจ
- การประเมินการทำงานของไต
- การตรวจระบบตับและทางเดินน้ำดี
- การตรวจการระบายอากาศและการไหลเวียนเลือดปอด
- การทำ sentinel lymph node mapping
- การตรวจต่อมไทรอยด์และต่อมน้ำลาย
ดังนั้น การตรวจสแกนกระดูกจึงเป็นเพียงหนึ่งในหลายการประยุกต์ใช้หลักของแพลตฟอร์ม Tc-99m มิใช่จุดมุ่งหมายเพียงประการเดียวของระบบนี้
3. แพลตฟอร์ม F-18 PET: ระบบการสร้างภาพระดับโมเลกุลแบบไซโคลตรอนเป็นฐาน
3.1 คุณสมบัติพื้นฐานของ F-18 และความเหมาะสมต่อการสร้างภาพด้วย PET
ฟลูออรีน-18 (Fluorine-18; F-18) เป็นไอโซโทปกัมมันตรังสีชนิดปล่อยโพซิตรอนที่ถูกใช้แพร่หลายที่สุดในระบบ PET เนื่องจากมีคุณสมบัติทางกายภาพที่เหมาะสมอย่างยิ่งต่อการสร้างภาพระดับโมเลกุลความละเอียดสูง
F-18 มีครึ่งชีวิตประมาณ 109.8 นาที ซึ่งยาวพอสำหรับการสังเคราะห์สารเภสัชรังสี การควบคุมคุณภาพ และการขนส่งในระดับภูมิภาค แต่ยังสั้นพอที่จะจำกัดปริมาณรังสีต่อผู้ป่วยให้อยู่ในระดับเหมาะสม
F-18 ปล่อยโพซิตรอนด้วยพลังงานสูงสุดประมาณ 0.635 MeV ซึ่งต่ำกว่า positron emitters หลายชนิด ส่งผลให้ระยะการเคลื่อนที่ของโพซิตรอนในเนื้อเยื่อก่อนการทำลายล้างสั้นลง จึงช่วยเพิ่มความแม่นยำเชิงตำแหน่งและความละเอียดของภาพ
คุณสมบัติเหล่านี้ทำให้ F-18 เป็นไอโซโทปหลักสำหรับงานสร้างภาพระดับโมเลกุลทั้งในทางคลินิกและการวิจัย
3.2 การผลิต F-18 ด้วยไซโคลตรอนและข้อกำหนดด้านโครงสร้างพื้นฐาน
แตกต่างจาก Tc-99m ที่สามารถใช้ระบบเครื่องกำเนิดรังสี F-18 ต้องผลิตโดยตรงด้วยเครื่องไซโคลตรอนผ่านปฏิกิริยานิวเคลียร์โดยใช้โปรตอนยิงเป้าน้ำออกซิเจน-18 เสริมเพิ่มสัดส่วน (Enriched [18O] Water Target)
ผลิตผ่านปฏิกิริยา
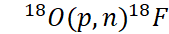
กระบวนการผลิต F-18 ต้องอาศัยโครงสร้างพื้นฐานที่ซับซ้อนกว่าระบบ Tc-99m อย่างมาก ได้แก่
- เครื่องไซโคลตรอนทางการแพทย์ (Medical Cyclotron)
- ระบบเป้าและระบบจัดการความร้อน
- ตู้ป้องกันรังสีสำหรับปฏิบัติงาน (Hot Cells)
- ระบบชุดสังเคราะห์สารอัตโนมัติ (Automated Synthesis Modules)
- ห้องปฏิบัติการควบคุมคุณภาพสารเภสัชรังสี
- สภาพแวดล้อมการผลิตตามหลักเกณฑ์วิธีการที่ดีในการผลิตยา (GMP)
ดังนั้น การดำเนินงานของแพลตฟอร์ม F-18 PET จึงต้องอาศัยทีมสหสาขาวิชาชีพที่มีความเชี่ยวชาญเฉพาะทางจำนวนมาก
ตัวอย่างสำหรับการเตรียมสาร F-18 สำหรับตรวจระบบกระดูก ใช้
ซึ่งเป็นฟลูออไรด์ไอออน (Fluoride Ion) ที่สามารถแลกเปลี่ยนกับหมู่ไฮดรอกซิล (Hydroxyl Group) ในผลึกไฮดรอกซีอะพาไทต์ เกิดการจับยึดลักษณะคล้ายฟลูออราอะพาไทต์ (Fluorapatite-like Binding) ที่ผิวกระดูก
3.3 หลักการสร้างภาพด้วย PET และข้อได้เปรียบของระบบตรวจวัด
PET แตกต่างจาก gamma camera/SPECT โดยพื้นฐานในเชิงฟิสิกส์ของการตรวจวัด
เมื่อ F-18 สลายตัว จะปล่อยโพซิตรอนซึ่งเคลื่อนที่ในเนื้อเยื่อก่อนทำลายล้างกับอิเล็กตรอน เกิดเป็นโฟตอนพลังงาน 511 keV สองตัวที่ปล่อยออกในทิศทางเกือบตรงข้ามกัน
ระบบ PET ตรวจจับโฟตอนทั้งสองพร้อมกันด้วยหลักการ coincidence detection และใช้ข้อมูลดังกล่าวสร้างแนวตอบสนองของเหตุการณ์การสลายตัว
ข้อได้เปรียบสำคัญของ PET คือไม่ต้องใช้ collimator เช่นใน gamma camera/SPECT จึงใช้โฟตอนได้อย่างมีประสิทธิภาพกว่ามาก ส่งผลให้มี
- ความไวในการตรวจวัดสูงกว่า (Higher Sensitivity)
- ความละเอียดเชิงพื้นที่สูงกว่า (Higher Spatial Resolution)
- ไม่ต้องใช้ตัวบีบนำทิศทางลำรังสี (Collimator)
- ความสามารถในการวิเคราะห์เชิงปริมาณสูงกว่า (Quantification) เช่น ค่าเอสยูวี (Standardized Uptake Value; SUV)
อย่างไรก็ตาม PET ยังมีข้อจำกัดทางฟิสิกส์ของตนเอง เช่น positron range, non-collinearity และข้อจำกัดของ timing resolution
3.4 บทบาทหลักของแพลตฟอร์ม PET ในเวชศาสตร์นิวเคลียร์สมัยใหม่
แม้ PET จะสามารถประยุกต์ใช้ในการตรวจสแกนกระดูกได้ แต่ PET มิได้ถูกพัฒนาขึ้นโดยมีเป้าหมายหลักเพื่อการตรวจสแกนกระดูก หากแต่ถูกพัฒนาเพื่อรองรับงานสร้างภาพระดับเมแทบอลิซึมและระดับโมเลกุลที่เกินขีดความสามารถของเวชศาสตร์นิวเคลียร์แบบดั้งเดิม
การประยุกต์ใช้ทางคลินิกที่สำคัญที่สุดคือ F-18 FDG PET ซึ่งเป็นเครื่องมือหลักในเวชศาสตร์มะเร็งวิทยาสมัยใหม่สำหรับ
- การแบ่งระยะโรคมะเร็ง
- การประเมินการแพร่กระจายของโรค
- การติดตามผลการรักษา
- การตรวจหาการกลับเป็นซ้ำของโรค
PET ยังมีบทบาทสำคัญใน
- การสร้างภาพสมอง
- การสร้างภาพเมแทบอลิซึมหัวใจ
- การตรวจการอักเสบ
- การสร้างภาพตัวรับและวิถีโมเลกุลจำเพาะ
ดังนั้น PET ควรถูกมองเป็นแพลตฟอร์มการสร้างภาพระดับโมเลกุลขั้นสูง มากกว่าจะเป็นเทคโนโลยีเฉพาะสำหรับการตรวจสแกนกระดูก
3.5 การประยุกต์ใช้ F-18 PET ในการตรวจสแกนกระดูก
สำหรับการตรวจสแกนกระดูก PET นิยมใช้ F-18 Sodium Fluoride (F-18 NaF) ซึ่งสะสมในกระดูกผ่านการแลกเปลี่ยนฟลูออไรด์ไอออนกับหมู่ไฮดรอกซิลในผลึกไฮดรอกซีอะพาไทต์ เกิดเป็นการจับแบบ fluorapatite-like binding ที่พื้นผิวกระดูก
กลไกนี้ทำให้ F-18 NaF มีความไวสูงต่อบริเวณที่มี osteoblastic activity และ bone remodeling สูง
อย่างไรก็ตาม ในระบบสุขภาพจริง F-18 NaF PET มักถูกใช้เป็นการประยุกต์เพิ่มเติมของโครงสร้างพื้นฐาน PET ที่มีอยู่แล้ว มากกว่าจะเป็นเหตุผลหลักในการติดตั้งระบบ PET เพื่อรองรับการตรวจสแกนกระดูกโดยเฉพาะ
ดังนั้น F-18 NaF PET จึงควรถูกมองเป็นการประยุกต์ใช้เฉพาะทางด้านกระดูกของแพลตฟอร์ม PET ที่กว้างกว่า มิใช่เทคโนโลยีการตรวจสแกนกระดูกที่ถูกพัฒนาขึ้นอย่างอิสระ
4. การสร้างภาพระบบกระดูกในฐานะกรณีศึกษาเชิงเปรียบเทียบของแพลตฟอร์ม Tc-99m และ F-18 PET
การสร้างภาพระบบกระดูกเป็นกรณีศึกษาที่เหมาะสมสำหรับการเปรียบเทียบแพลตฟอร์ม Tc-99m และ F-18 PET เนื่องจากทั้งสองระบบสามารถใช้ประเมินกระบวนการทางสรีรวิทยาของกระดูกที่ใกล้เคียงกันได้ ขณะเดียวกันก็อาศัยสถาปัตยกรรมการผลิตไอโซโทป ฟิสิกส์การตรวจวัด และโครงสร้างพื้นฐานทางคลินิกที่แตกต่างกันโดยพื้นฐาน
ในบริบทนี้ การเปรียบเทียบระหว่าง Tc-99m Bone Scintigraphy และ F-18 NaF PET มิได้มีวัตถุประสงค์เพื่อระบุว่าเทคโนโลยีใด “เหนือกว่า” โดยสัมบูรณ์ หากแต่เพื่อแสดงให้เห็นว่าความแตกต่างของสถาปัตยกรรมแพลตฟอร์มเวชศาสตร์นิวเคลียร์นำไปสู่ความแตกต่างด้านสมรรถนะ ข้อจำกัดในการดำเนินงาน และยุทธศาสตร์การใช้งานทางคลินิกอย่างไร
4.1 Tc-99m Bone Scintigraphy: การประยุกต์ใช้แพลตฟอร์มเวชศาสตร์นิวเคลียร์แบบดั้งเดิมสำหรับการประเมินระบบกระดูก
Tc-99m Bone Scintigraphy เป็นหนึ่งในการประยุกต์ใช้ที่แพร่หลายที่สุดของแพลตฟอร์ม Tc-99m โดยทั่วไปใช้สารเภสัชรังสีกลุ่มฟอสโฟเนต เช่น Tc-99m MDP, Tc-99m HDP และ Tc-99m HMDP ซึ่งจับกับพื้นผิวผลึกไฮดรอกซีอะพาไทต์ในกระดูก โดยเฉพาะบริเวณที่มีการสร้างกระดูกใหม่หรือมี osteoblastic activity สูง
ดังนั้น การสะสมของสารเภสัชรังสีในภาพจึงสะท้อนกิจกรรมของกระบวนการ bone remodeling มากกว่าการแสดงโครงสร้างทางกายวิภาคของกระดูกโดยตรง
คุณลักษณะดังกล่าวทำให้ Tc-99m Bone Scintigraphy มีความไวสูงต่อพยาธิสภาพที่เกี่ยวข้องกับการเปลี่ยนแปลงของ bone turnover เช่น การแพร่กระจายของมะเร็งไปยังกระดูก การติดเชื้อกระดูก การบาดเจ็บจาก stress fracture และโรคกระดูกจากความผิดปกติของเมแทบอลิซึม
ด้วยต้นทุนที่เหมาะสม ความพร้อมใช้งานสูง และความสามารถในการรองรับผู้ป่วยจำนวนมาก Tc-99m Bone Scintigraphy จึงกลายเป็นมาตรฐานสำหรับการตรวจสแกนกระดูกในเวชปฏิบัติประจำวันของหลายระบบสุขภาพ
4.2 F-18 NaF PET Bone Imaging: การประยุกต์ใช้แพลตฟอร์มการสร้างภาพระดับโมเลกุลสำหรับการประเมินระบบกระดูก
F-18 NaF PET เป็นการประยุกต์ใช้แพลตฟอร์ม PET ในการตรวจสแกนกระดูก โดยใช้ F-18 Sodium Fluoride ซึ่งสะสมในกระดูกผ่านการแลกเปลี่ยนฟลูออไรด์ไอออนกับหมู่ไฮดรอกซิลในผลึกไฮดรอกซีอะพาไทต์
กลไกดังกล่าวทำให้ F-18 NaF มีความไวสูงต่อบริเวณที่มี osteoblastic activity สูงในลักษณะคล้ายกับสาร bone-seeking agents ของ Tc-99m อย่างไรก็ตาม เมื่อใช้ร่วมกับแพลตฟอร์ม PET ซึ่งมีสมรรถนะการตรวจวัดที่เหนือกว่า จึงทำให้สามารถสร้างภาพระบบกระดูกได้ด้วยความไวและความละเอียดเชิงพื้นที่ที่สูงกว่า
ในทางคลินิก F-18 NaF PET มักถูกใช้ในสถานการณ์ที่ต้องการเพิ่ม sensitivity หรือ specificity ในการประเมินรอยโรคของกระดูก เช่น การประเมิน metastatic bone disease ที่ซับซ้อน กรณีผล bone scintigraphy ไม่ชัดเจน หรือการติดตามผลเชิงปริมาณในงานวิจัยและเวชศาสตร์แม่นยำ
อย่างไรก็ตาม การใช้งานดังกล่าวโดยทั่วไปเกิดขึ้นในศูนย์ที่มีโครงสร้างพื้นฐาน PET อยู่แล้ว มากกว่าการลงทุนติดตั้งระบบ PET เพื่อรองรับการตรวจสแกนกระดูกโดยเฉพาะ
4.3 การเปรียบเทียบสมรรถนะเชิงฟิสิกส์ของ Bone Scintigraphy และ Bone PET
แม้ว่าทั้งสองเทคโนโลยีจะใช้ประเมินกระบวนการ bone remodeling ที่คล้ายคลึงกัน แต่สมรรถนะของภาพที่ได้แตกต่างกันอย่างมีนัยสำคัญเนื่องจากฟิสิกส์พื้นฐานของระบบตรวจวัดที่แตกต่างกัน
Tc-99m Bone Scintigraphy อาศัยการตรวจวัดโฟตอนแกมมาผ่าน collimator ซึ่งเป็นข้อจำกัดพื้นฐานของระบบ gamma camera/SPECT เนื่องจากโฟตอนส่วนใหญ่ต้องถูกปฏิเสธเพื่อรักษาข้อมูลเชิงตำแหน่ง ส่งผลให้ประสิทธิภาพการตรวจวัดลดลงอย่างมาก
ความละเอียดเชิงพื้นที่ของระบบยังถูกจำกัดเพิ่มเติมโดยเรขาคณิตของ collimator ระยะห่างระหว่าง detector กับผู้ป่วย การทะลุผ่านผนังกั้นของ collimator และการกระเจิงของโฟตอน
ในทางตรงกันข้าม PET ใช้ coincidence detection โดยไม่ต้องใช้ collimator จึงมีความไวในการตรวจวัดและความละเอียดเชิงพื้นที่สูงกว่าโดยธรรมชาติ อีกทั้งยังรองรับการวิเคราะห์เชิงปริมาณผ่านตัวชี้วัด เช่น Standardized Uptake Value (SUV)
ดังนั้น ในมุมมองของ detector physics F-18 NaF PET จึงมีข้อได้เปรียบเหนือกว่า Tc-99m Bone Scintigraphy อย่างชัดเจนในด้านความสามารถในการตรวจพบรอยโรค ความละเอียดเชิงพื้นที่ และการวิเคราะห์เชิงปริมาณ
อย่างไรก็ตาม ข้อได้เปรียบดังกล่าวสะท้อนสมรรถนะของ detector platform มิได้หมายความว่า PET เหนือกว่าทางคลินิกในทุกบริบท
5. การเปรียบเทียบเชิงโครงสร้างพื้นฐานและห่วงโซ่อุปทานของทั้งสองแพลตฟอร์ม
นอกเหนือจากสมรรถนะของการสร้างภาพ ความแตกต่างที่สำคัญที่สุดประการหนึ่งระหว่างแพลตฟอร์ม Tc-99m และ F-18 PET อยู่ที่สถาปัตยกรรมของโครงสร้างพื้นฐานและห่วงโซ่อุปทานที่รองรับการดำเนินงานของแต่ละระบบ
แพลตฟอร์ม Tc-99m ใช้รูปแบบการผลิตแบบศูนย์กลางและกระจายการใช้งานสู่หน่วยบริการปลายทาง โดย Mo-99 ถูกผลิตในเครื่องปฏิกรณ์นิวเคลียร์ระดับประเทศหรือระดับภูมิภาค และกระจายสู่โรงพยาบาลในรูปเครื่องกำเนิดรังสี ทำให้สามารถเตรียม Tc-99m ณ จุดบริการได้
ในทางตรงกันข้าม แพลตฟอร์ม F-18 PET ต้องอาศัยเครือข่ายการผลิตระดับภูมิภาคที่ประกอบด้วยศูนย์ไซโคลตรอน ห้องสังเคราะห์สารเภสัชรังสี ระบบควบคุมคุณภาพ และระบบขนส่งเร่งด่วนที่ดำเนินการภายใต้ข้อจำกัดของครึ่งชีวิตสั้นของไอโซโทป
ดังนั้น Tc-99m และ F-18 PET จึงเป็นตัวแทนของสถาปัตยกรรมระบบบริการสุขภาพที่แตกต่างกันโดยพื้นฐาน ทั้งในด้านระดับการรวมศูนย์ ความซับซ้อนของการดำเนินงาน และข้อกำหนดด้านโครงสร้างพื้นฐาน
6. การจัดสรรทรัพยากรและข้อพิจารณาด้านเศรษฐศาสตร์สุขภาพ
ในระบบสุขภาพจริง การเลือกใช้เทคโนโลยีเวชศาสตร์นิวเคลียร์มิได้ขึ้นกับสมรรถนะทางเทคนิคเพียงอย่างเดียว หากแต่ขึ้นกับความสมดุลระหว่างต้นทุนและคุณค่าทางคลินิกที่ได้รับ
แพลตฟอร์ม Tc-99m มีข้อได้เปรียบด้านเศรษฐศาสตร์สุขภาพอย่างชัดเจน เนื่องจากใช้โครงสร้างพื้นฐานต่ำกว่า มี workflow ด้าน radiopharmacy ที่ง่ายกว่า ใช้บุคลากรเฉพาะทางน้อยกว่า และรองรับผู้ป่วยจำนวนมากได้ด้วยต้นทุนต่อการตรวจต่ำกว่า
ในทางตรงกันข้าม PET/CT เป็นทรัพยากรที่มีต้นทุนสูง ทั้งด้านเครื่องมือ โครงสร้างพื้นฐาน และค่าใช้จ่ายในการดำเนินงาน จึงมักถูกจัดสรรให้กับข้อบ่งชี้ทางคลินิกที่ molecular imaging ให้คุณค่าทางการแพทย์เพิ่มเติมอย่างมีนัยสำคัญ
ดังนั้น แม้ F-18 NaF PET จะให้สมรรถนะในการสร้างภาพระบบกระดูกที่เหนือกว่า แต่การใช้เป็นเครื่องมือ routine skeletal imaging สำหรับผู้ป่วยทั่วไปอาจไม่ใช่แนวทางที่มีประสิทธิภาพสูงสุดด้านการใช้ทรัพยากรในหลายระบบสุขภาพ
7. การออกแบบระบบเวชศาสตร์นิวเคลียร์แบบหลายระดับเชิงยุทธศาสตร์
จากความแตกต่างด้านสมรรถนะ โครงสร้างพื้นฐาน และต้นทุนดังกล่าว Tc-99m และ PET ไม่ควรถูกมองเป็นเทคโนโลยีที่แข่งขันกันโดยตรงภายในระบบสุขภาพ หากแต่ควรถูกมองเป็นองค์ประกอบที่เสริมกันภายใต้ระบบบริการเวชศาสตร์นิวเคลียร์แบบหลายระดับ
ภายใต้กรอบดังกล่าว แพลตฟอร์ม Tc-99m ทำหน้าที่เป็น แพลตฟอร์มสร้างภาพทางนิวเคลียร์หลักสำหรับการเข้าถึงในวงกว้าง รองรับงานตรวจทั่วไปที่มีปริมาณผู้ป่วยสูงและต้องการการเข้าถึงบริการอย่างแพร่หลาย
ในขณะที่แพลตฟอร์ม PET ทำหน้าที่เป็น แพลตฟอร์ม molecular imaging ขั้นสูงสำหรับการส่งต่อเฉพาะทาง รองรับการตรวจที่ต้องการความไว ความจำเพาะ หรือความสามารถเชิงปริมาณที่สูงกว่า
ภายใต้กรอบนี้ F-18 NaF PET จึงควรถูกจัดวางให้เป็น advanced skeletal imaging application ของแพลตฟอร์ม PET มากกว่าการเป็นเทคโนโลยีทดแทน Tc-99m Bone Scintigraphy โดยตรง
8. บทสรุป
Tc-99m และ F-18 PET ไม่ควรถูกมองเพียงว่าเป็นไอโซโทปกัมมันตรังสีสองชนิดสำหรับการสร้างภาพทางเวชศาสตร์นิวเคลียร์ หากแต่ควรถูกมองว่าเป็นตัวแทนของสองสถาปัตยกรรมหลักของระบบเวชศาสตร์นิวเคลียร์สมัยใหม่ที่มีปรัชญาการออกแบบแตกต่างกันโดยพื้นฐาน
แพลตฟอร์ม Tc-99m สะท้อนแนวคิดของระบบสร้างภาพแบบกระจายศูนย์ที่ได้รับการปรับให้เหมาะสมต่อการเข้าถึงบริการในวงกว้าง ความคุ้มค่า และการรองรับภาระงานทางคลินิกจำนวนมาก
ในทางตรงกันข้าม แพลตฟอร์ม F-18 PET สะท้อนแนวคิดของระบบ molecular imaging ขั้นสูงที่ได้รับการปรับให้เหมาะสมต่อสมรรถนะการสร้างภาพ ความไวในการตรวจวัด และความสามารถในการวิเคราะห์เชิงปริมาณ ภายใต้สภาพแวดล้อมทางคลินิกที่มีความเฉพาะทางและต้องใช้โครงสร้างพื้นฐานเข้มข้นกว่า
กรณีศึกษาการสร้างภาพระบบกระดูกแสดงให้เห็นว่า แม้ F-18 NaF PET จะมีสมรรถนะทางฟิสิกส์เหนือกว่า Tc-99m Bone Scintigraphy ในหลายด้าน แต่ข้อได้เปรียบดังกล่าวมิได้หมายความว่า PET ถูกออกแบบมาเพื่อทดแทนแพลตฟอร์ม Tc-99m สำหรับการตรวจสแกนกระดูก หากแต่สะท้อนว่าการตรวจสแกนกระดูกเป็นเพียงหนึ่งในหลายการประยุกต์ใช้เฉพาะทางของแพลตฟอร์ม PET ที่กว้างกว่ามาก
ดังนั้น การเปรียบเทียบ Tc-99m Bone Scintigraphy และ F-18 NaF PET ควรถูกตีความว่าเป็นการเปรียบเทียบระหว่างการประยุกต์ใช้ด้านระบบกระดูกของสองแพลตฟอร์มเวชศาสตร์นิวเคลียร์ที่มีสถาปัตยกรรมแตกต่างกันโดยพื้นฐาน มากกว่าการเป็นการแข่งขันเชิงเทคโนโลยีโดยตรงระหว่างเทคนิคการตรวจสแกนกระดูกสองชนิด
*************************************************
Suggested References
- Cherry SR, Sorenson JA, Phelps ME. Physics in Nuclear Medicine. 5th ed. Elsevier.
- IAEA. Cyclotron Produced Radionuclides: Principles and Practice.
- IAEA. Technetium-99m Radiopharmaceuticals: Manufacture of Kits.
- Knoll GF. Radiation Detection and Measurement. 4th ed.
- Wagner HN, Szabo Z, Buchanan JW. Principles of Nuclear Medicine.
ใส่ความเห็น